每周医药看点(2月17日—23日)
- 2025-03-06 08:40
- 作者:刘鹤
- 来源:中国食品药品网
2025年全国药品注册管理和上市后监管工作会议在山东省济南市召开;国家药监局公布药品说明书适老化及无障碍改革试点名单(第四批)……2月17日—23日,医药行业的这些动态值得关注。
行业政策及药监动态
1.2025年全国药品注册管理和上市后监管工作会议在山东省济南市召开。会议总结2024年工作,分析当前形势,研究部署2025年重点任务。国家药监局药品注册司和药品监管司主要负责同志分别就2025年药品注册管理和上市后监管重点工作进行具体安排。
2.国家药监局公布药品说明书适老化及无障碍改革试点名单(第四批),替格瑞洛片等415个品种列入其中。
3.国家药监局发布公告,复方公英胶囊由处方药转换为非处方药。品种名单及非处方药说明书范本一并发布。按照品种名单,规格为每粒装0.28克的复方公英胶囊转换为甲类非处方药,且为处方药和非处方药双跨品种。
4.国家药监局药品审评中心(CDE)发布公告,将北京凯莱天成医药科技有限公司的酒石酸艾格司他胶囊纳入《以患者为中心的罕见疾病药物研发试点工作计划(“关爱计划”)》试点项目。
5.CDE网站公示9个仿制药一致性评价任务,涉及盐酸林可霉素注射液等品种。
产品研发上市信息
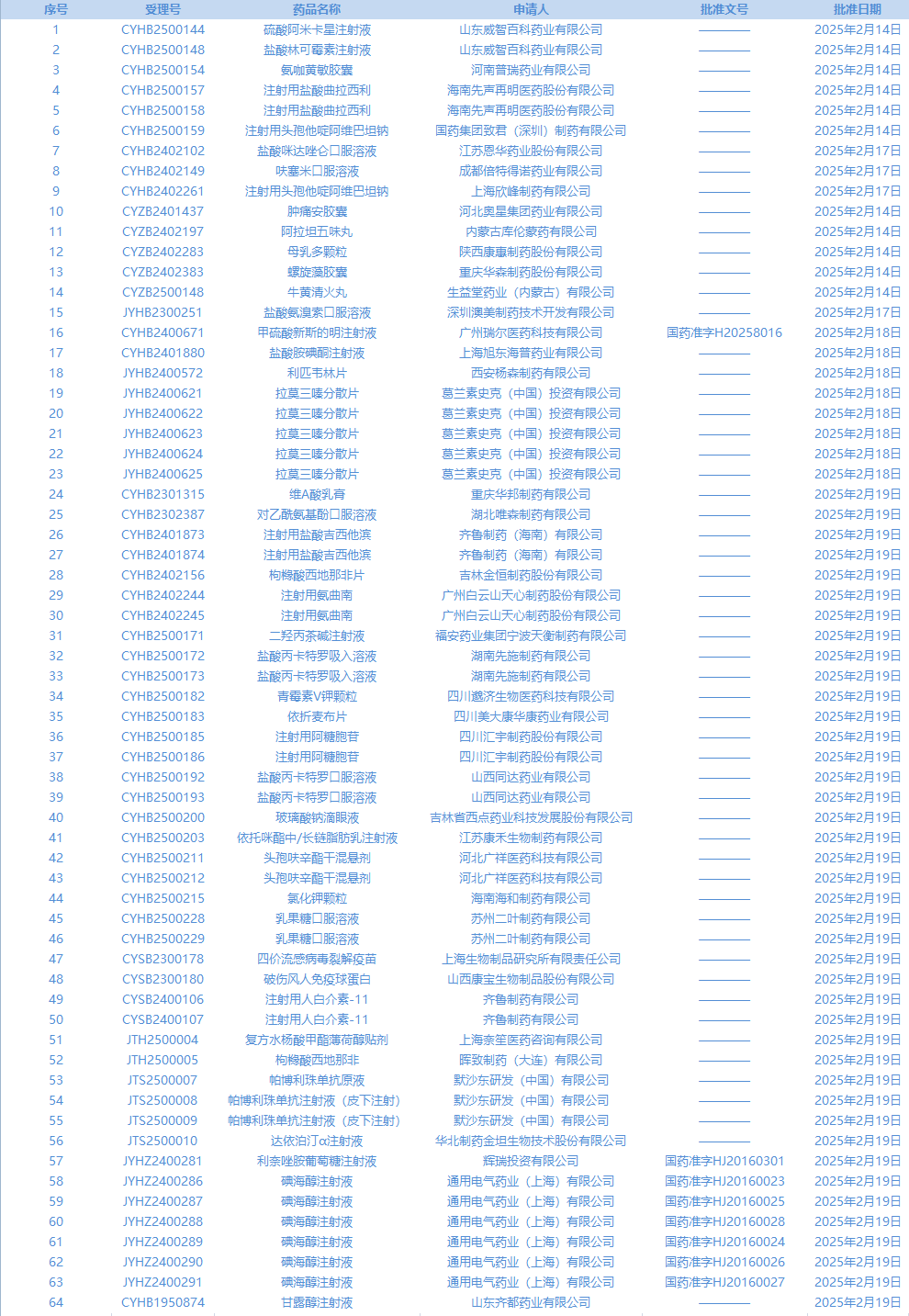
1.国家药监局发布5期药品批准证明文件送达信息,共包括64个受理号,涉及山东齐都药业有限公司等企业。
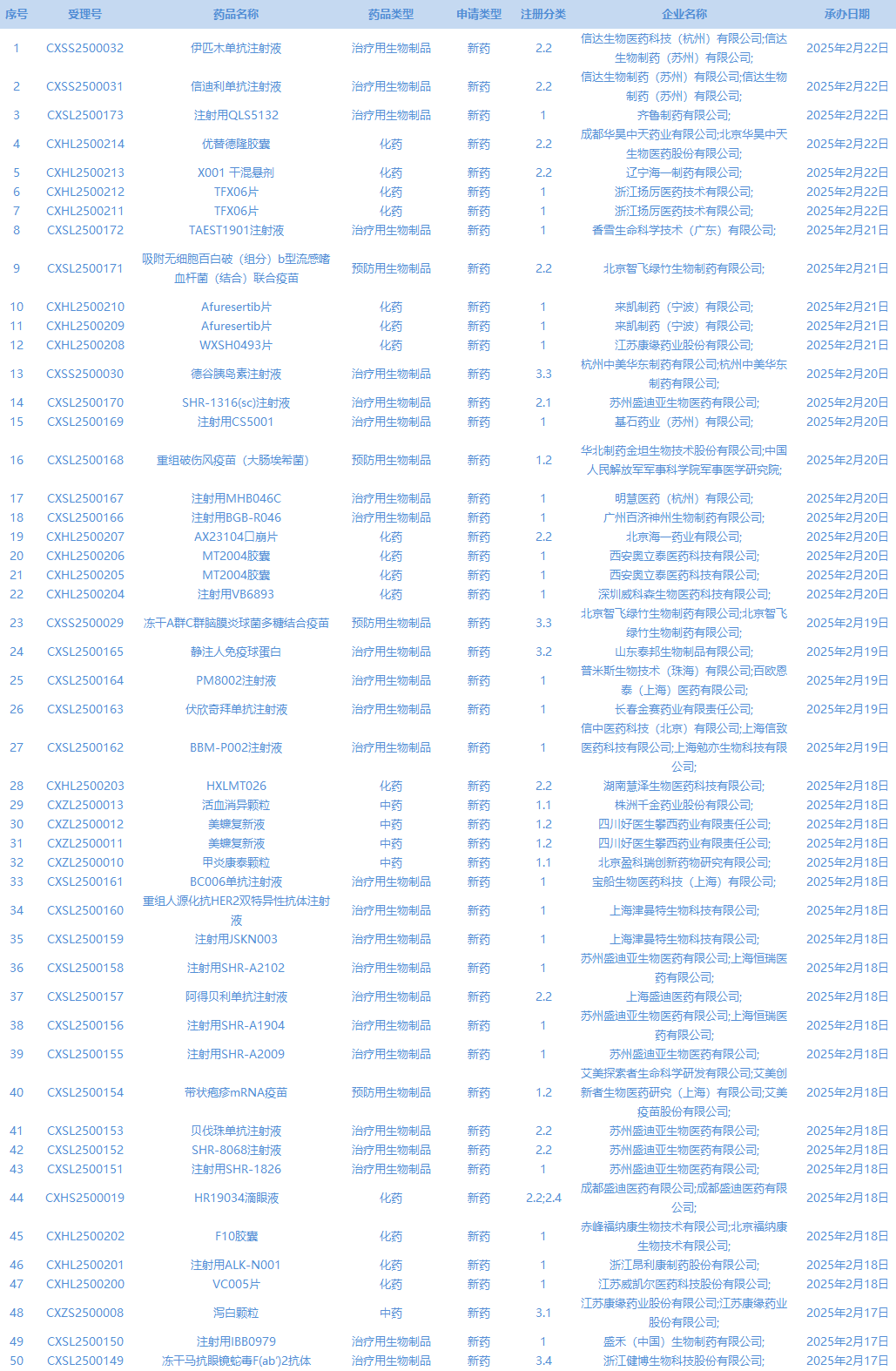
2.CDE承办受理50个新药上市申请,包括伊匹木单抗注射液等。
3.万邦德发布公告称,公司全资子公司万邦德制药集团有限公司收到美国食品药品管理局(FDA)的认定函,甲钴胺用于治疗肌萎缩侧索硬化(ALS)获得FDA授予的孤儿药资格认定。
4.信达生物宣布,公司PD-1/IL-2α-bias双特异性抗体融合蛋白IBI363获得FDA授予快速通道资格,拟定适应证为抗PD-(L)1免疫检查点抑制剂及含铂化疗治疗后进展的局部晚期或转移性鳞状非小细胞肺癌。
5.跃赛生物宣布,公司自主研发的针对帕金森病的自体诱导多能干细胞(iPSC)衍生细胞药物UX-DA001注射液新药临床试验申请获得FDA正式批准。据悉,UX-DA001已在2024年12月获得CDE临床试验默示许可。
医药企业观察
1.和铂医药宣布与英矽智能达成战略合作,双方将利用各自在抗体发现与人工智能领域的技术优势,加速新型治疗性抗体的研发进程。根据合作协议,双方将结合和铂医药行业领先的技术平台、专有数据集以及在抗体开发领域的丰富经验,与英矽智能在构建一体化AI驱动药物研发平台方面的技术优势,共同推进AI赋能的抗体发现算法和应用开发。
2.珂阑医药宣布完成超亿元A+轮融资,本轮融资由国投创业基金领投。融资资金将主要用于加速推进多个核心管线进入临床申报和开发,以及研发平台和团队的拓展。
3.九州通宣布与达因药业签署2025战略合作协议。根据协议,双方将整合九州通的高效分销网络以及达因药业在儿科用药及健康产品上的研发优势,围绕达因药业产品线深化合作,在深度分销、电商配送、核心连锁配送、广阔市场覆盖、医院配送及重点项目协同等领域展开全方位战略联动。
4.贝海生物宣布已与Zydus Lifesciences达成重大战略合作,授予其新药BEIZRAY在美国市场的独家商业化权益。根据协议条款,贝海生物将负责该产品的生产和供应,Zydus Lifesciences美国子公司Zydus Pharmaceutical s(USA)将负责该产品在美国的商业化。本次合作标志着贝海生物在国际化战略上迈出了关键性一步。
药品集中采购
1.全国中成药联合采购办公室公示全国中成药采购联盟集中采购复活拟中选及非报价代表品拟中选结果,8个药品获得复活拟中选资格,包括清开灵注射液、丹参片、双黄连注射液等;134个非报价代表品拟中选,涉及血脂康胶囊、活血通脉胶囊、三七通舒胶囊等。
2.广东省药品交易中心公布广东联盟金莲花胶囊等中成药集中带量采购中选结果,共有来自上海皇象铁力蓝天制药有限公司等企业的323个产品中选。(刘鹤整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:周雨同)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐