每周医药看点(7月22日—7月28日)
- 2024-07-30 08:54
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 国家医保局发布《2023年全国医疗保障事业发展统计公报》;国家药监局药品审评中心(CDE)就《多糖结合疫苗质量控制技术指导原则(征求意见稿)》《模型引导的创新药物剂量探索和优化技术指导原则(征求意见稿)》等文件公开征求意见……7月22日—7月28日,医药行业的这些动态值得关注。
行业政策动态
1.国家医保局发布《2023年全国医疗保障事业发展统计公报》。公报显示,2023年,全国基本医疗保险(含生育保险)基金总收入比上年增长8.3%;通过谈判降价和医保报销,当年累计为患者减负近2300亿元。
2.国家医保局办公室发布《国家医疗保障局办公室关于印发按病组和病种分值付费2.0版分组方案并深入推进相关工作的通知》(以下简称《通知》)。《通知》要求做好2.0版分组落地执行工作,同时强调对因住院时间长、医疗费用高、新药耗新技术使用、复杂危重症或多学科联合诊疗等不适合按DRG/DIP标准支付的病例,医疗机构可自主申报特例单议。
3.CDE就《多糖结合疫苗质量控制技术指导原则(征求意见稿)》《模型引导的创新药物剂量探索和优化技术指导原则(征求意见稿)》《化药口服固体制剂中间产品/待包装产品存放时限研究技术指导原则(征求意见稿)》《发酵或半合成化学仿制药抗生素有关物质限度制定指导原则(征求意见稿)》《已上市化药药品补充申请药学自评估报告(原料药/制剂)(征求意见稿)》公开征求意见,征求意见时限为自文件发布之日起1个月。
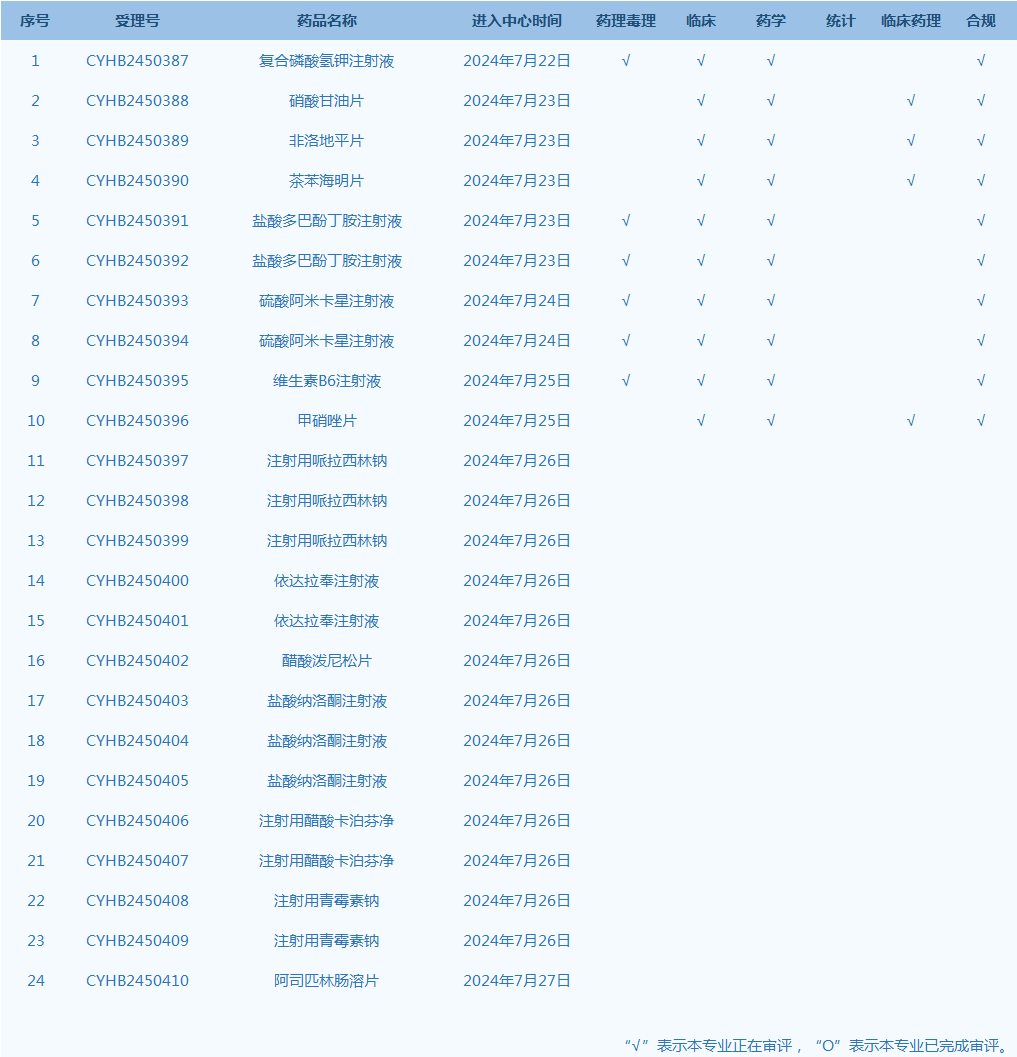
4.CDE网站公示24个仿制药一致性评价任务,涉及复合磷酸氢钾注射液等品种(截至7月28日)。
产品研发上市信息
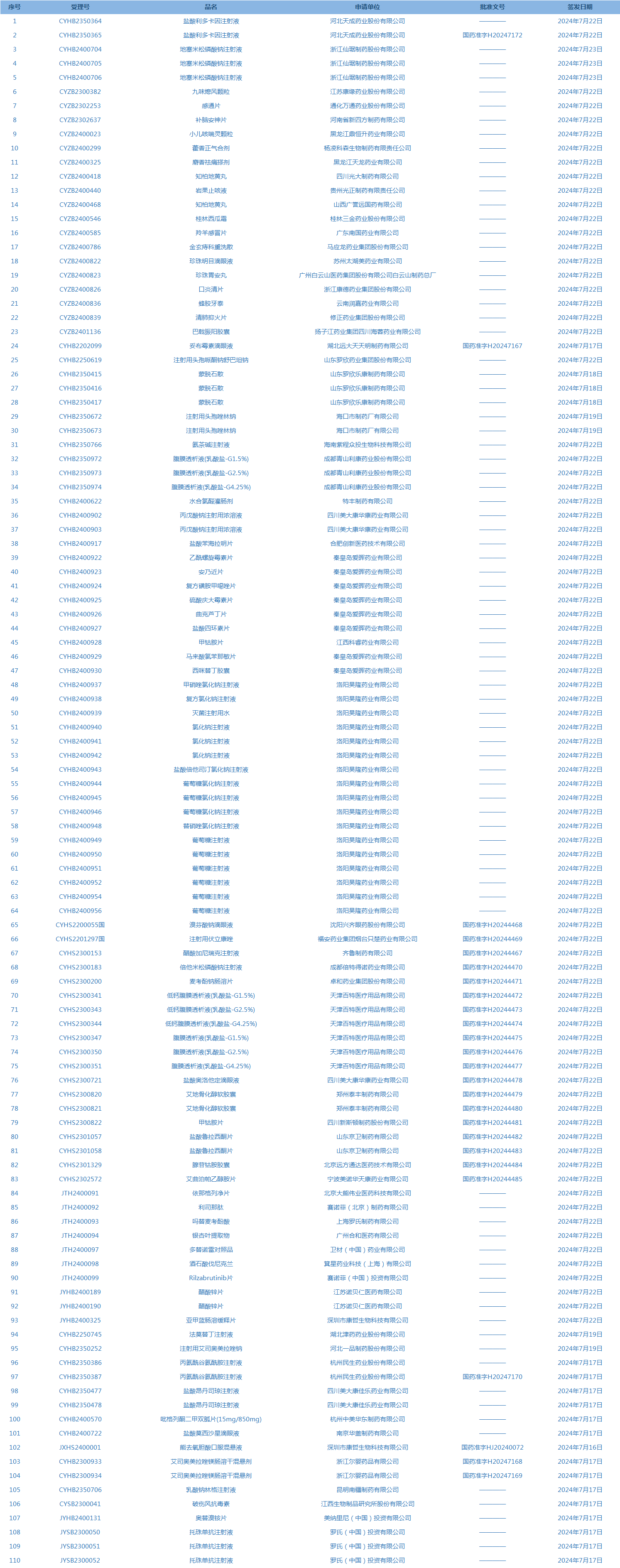
1.国家药监局发布4期药品批准证明文件送达信息,共包括110个受理号,涉及罗氏(中国)投资有限公司等企业(截至7月28日)。
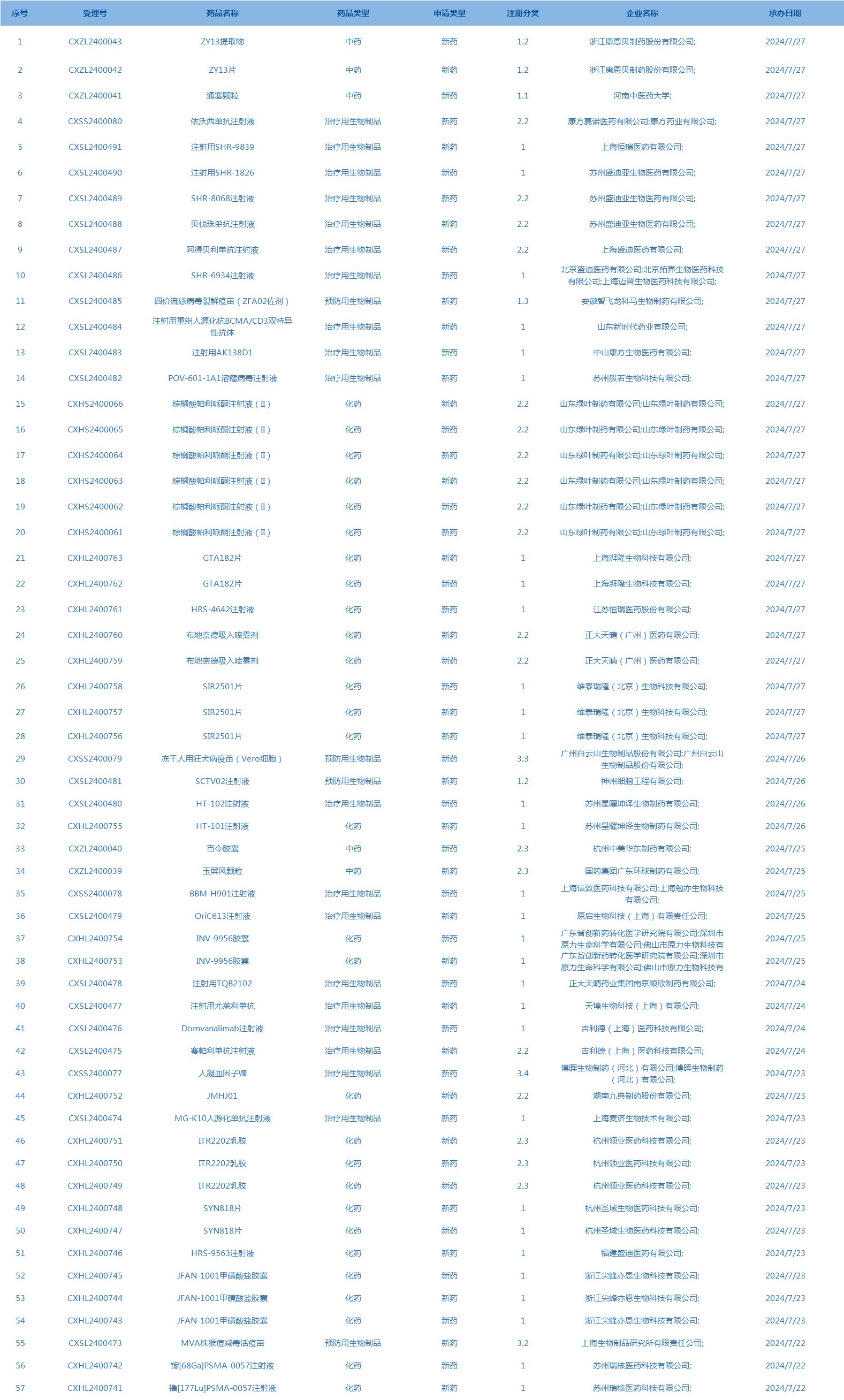
2.CDE承办受理57个新药上市申请,包括通塞颗粒等药品(截至7月28日)。
3.汇宇制药发布公告称,公司全资子公司Seacross Pharma(Europe) Ltd.收到爱尔兰健康产品监管局核准签发的公司产品注射用伏立康唑的上市许可,收到葡萄牙国家药品和健康产品管理局核准签发的公司产品唑来膦酸注射液的上市许可。
4.步长制药发布公告称,收到马来西亚药物管制局核准签发的药品注册证明文件,公司产品稳心颗粒符合马来西亚传统中药注册标准。
5.中美瑞康宣布,其自主研发的小激活RNA(saRNA)药物RAG-18获得美国食品药品管理局(FDA)的儿科罕见病药物资格(RPDD)。
6.康宁杰瑞宣布,公司自主研发的组织因子途径抑制物(TFPI)单克隆抗体KN057再次获得美国FDA授予的孤儿药资格,用于血友病B的治疗。
医药企业观察
1.华东医药发布公告称,全资子公司中美华东与公司参股的香港上市公司荃信生物签署QX005N产品的合作开发及市场推广服务协议。中美华东获得荃信生物QX005N产品在大中华区的排他共同合作开发权、独家市场推广的选择权及上市许可持有人转让的优先合作权。根据合作协议,中美华东与荃信生物将共同开展临床、非临床研究及注册相关工作,双方各承担商业化之前发生的临床开发及注册费的50%。若未来中美华东行使独家市场推广选择权,中美华东将负责QX005N产品在授权区域内的独家市场推广服务,荃信生物负责QX005N产品及临床试验样品的独家生产、供应及质量控制。
2.双成药业发布公告称,拟与公司关联方清普生物签订《技术服务合同》,清普生物委托公司开展QP002凝胶项目的技术研究,并支付技术服务经费和报酬480万元。
3.微光基因与濒湖生物宣布就探索新型DNA编辑工具在iPSC细胞领域的应用及产品开发达成专利许可协议。根据协议,濒湖生物获得微光基因自主研发的enCas12Ultra编辑蛋白在全球范围内商业化使用的非独家许可,用于iPSC细胞药物的开发及生产。
药品集中采购
1.河北省医用药品器械集中采购中心发布《关于开展集采同通用名药品竞价挂网的通知》。通知显示,该省将开展集采同通用名药品竞价挂网,申报范围为国采通用名药品、联盟集采及省采中选同通用名药品、国采中选同企业已过评未中选规格,以及未挂网原研、过评药品。
2.湖南省医保局发布通知,该省将在同时在8月1日执行国采第六批(胰岛素)专项接续、“陕西九省联盟”和“江西干扰素联盟”集采及京津冀“3+N”药品集采中选结果。值得注意的是,第六批国采胰岛素专项接续中选结果要执行“两票制”。其中,胰岛素专项接续采购周期自中选结果执行之日起至2027年12月31日;陕西九省联盟采购周期原则上自中选结果执行之日起至2025年12月31日,江西干扰素联盟采购周期原则上为4年,两批次第一协议年度执行时间均为2024年8月1日至2024年12月31日,其约定采购量按前期报量进行折算(按附件约定采购量×5/12);而京津冀“3+N”联盟采购周期为一年。采购周期内,如国家组织药品集中采购的药品与本次联盟带量采购的药品存在重复,按国家中选结果执行。
3.四川省医保局印发《四川省药械集中采购及医药价格监管平台挂网药品价格监测管理办法》(以下简称《办法》),自2024年8月25日起施行,有效期5年。《办法》显示,四川将根据平台挂网药品价格,按照价格比值分别划分为合理、异常、严重异常三个区间,对应进行绿色、黄色、红色标示,提醒医药企业、医疗机构规范价格和采购行为。凡在平台挂网的药品,其价格均纳入挂网药品价格监测范围,包括集中带量采购药品、价格联动采购药品和备案采购药品及要求监测管理的其他药品。(本报记者刘思慧整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:周雨同)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐