前沿新知 | 基因编辑技术开发现状和未来应用前景
- 2021-05-26 08:49
- 作者:郝世超
- 来源:中国食品药品网
2021年1月,博雅辑因针对输血依赖型β地中海贫血的CRISPR/Cas9基因编辑疗法产品ET-01的临床试验申请(IND)获国家药监局药品审评中心批准。ET-01疗法成为我国首个获批开展临床试验的基因编辑疗法产品和造血干细胞产品。
定义及分类
基因编辑是指对目标基因进行删除、替换、插入等操作,以获得新的功能或表型。基因编辑是生命医学领域的革命性技术,基因编辑技术的开发及应用使得生物体的遗传改造进入了前所未有的深度与广度,其临床转化也正在全球范围内高速推进。基因编辑技术主要可分为ZFN技术、TALEN技术、CRISPR/Cas技术及RNA编辑技术。

锌指核酸酶技术(Zinc Finger Nucleases,ZFNs)被称为第一代基因编辑技术。ZFNs技术的优势为基因修复方式多样、精准更换基因、对基因表达强度影响较小。ZFNs技术自问世至今因专利封锁无大规模应用,且无突破性进展。
转录激活子样效应子介导核酸酶技术(TALE Nucleases,TALENs),作为ZFNs技术的一种替代物迅速出现,TALENs技术用于基因组编辑和引入靶向DSBs。对于相同的靶点,TALENs有着与ZFNs相同的切割效率,但是毒性通常比ZFNs低,并且其构建也比ZFNs容易。
Cas9核酸内切酶相关的成簇的规律间隔的短回文重复序列(CRISPR-Cas9)技术是第三代基因编辑技术。CRISPR/Cas系统原本是细菌和古菌进化出来用于抵御外来病毒及质粒DNA的适应性免疫系统,目前研究最多、进展最快、应用最广的是第二大类中的II型(CRISPR/Cas9)。CRISPR-Cas9被Nature列为2013年年度十大科技进展之一。与ZFNs技术和TALENs技术相比,CRISPR系统是轻量级的基因编辑系统,并且CRISPR/Cas9的设计简单、成本低,对于相同的靶点,CRISPR/Cas9有相当甚至更好的靶向效率。
此外还有RNA编辑技术。DNA编辑是对遗传信息永久的改变,因此DNA编辑必须既安全又有效地进行。相比之下,RNA碱基编辑是可逆的,且编辑效果与剂量有关。RNA编辑技术提供了修复突变的新方法,正逐渐成为基因编辑技术重要的组成部分。
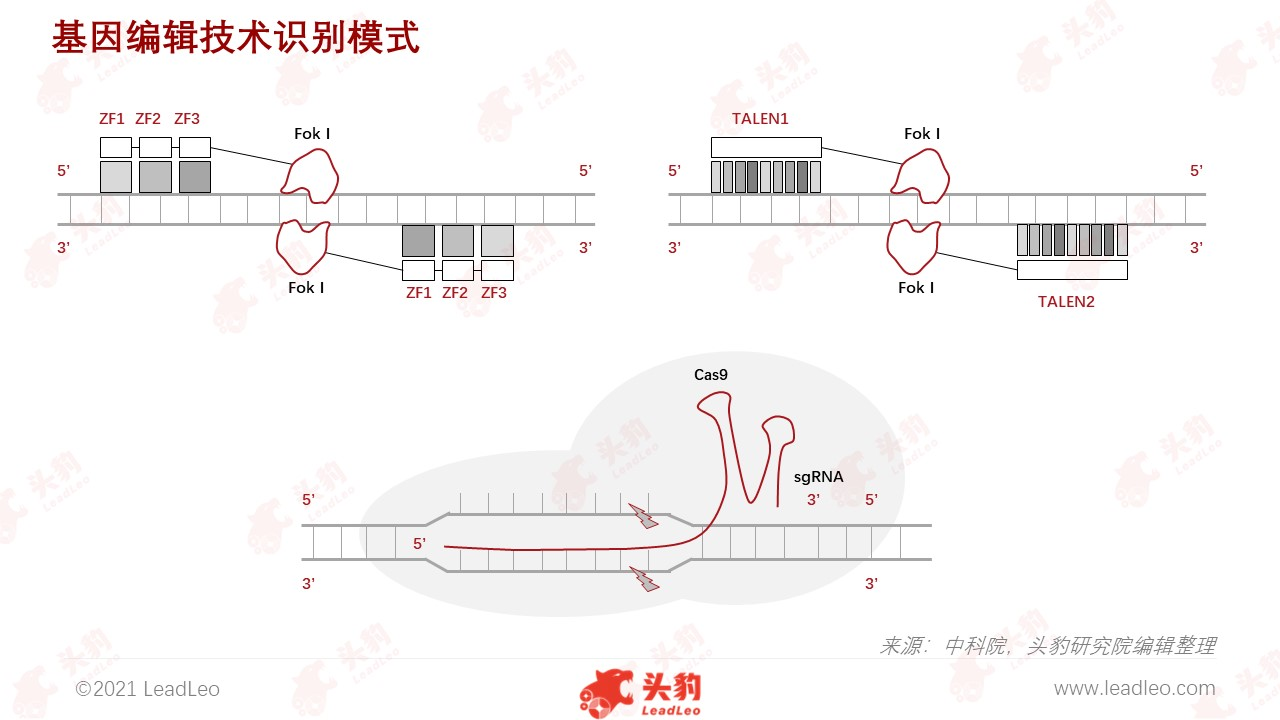
基因编辑技术在问世20年后尚未在临床上规模化应用,原因在于ZFNs技术受专利封锁,而TALENs技术和CRISPR/Cas9技术出现时间较短。虽然当下TALENs在临床上应用更广泛,但CRISPR/Cas9优势更突出,其系统设计简便、可实现多基因编辑。由于CRISPR/Cas9问世时间较短,评估其临床应用风险需要时日,但在未来CRISPR/Cas9切割元件的优化趋势下,以CRISPR/Cas9为代表的CRISPR技术或将主导基因编辑技术的未来。

应用潜力
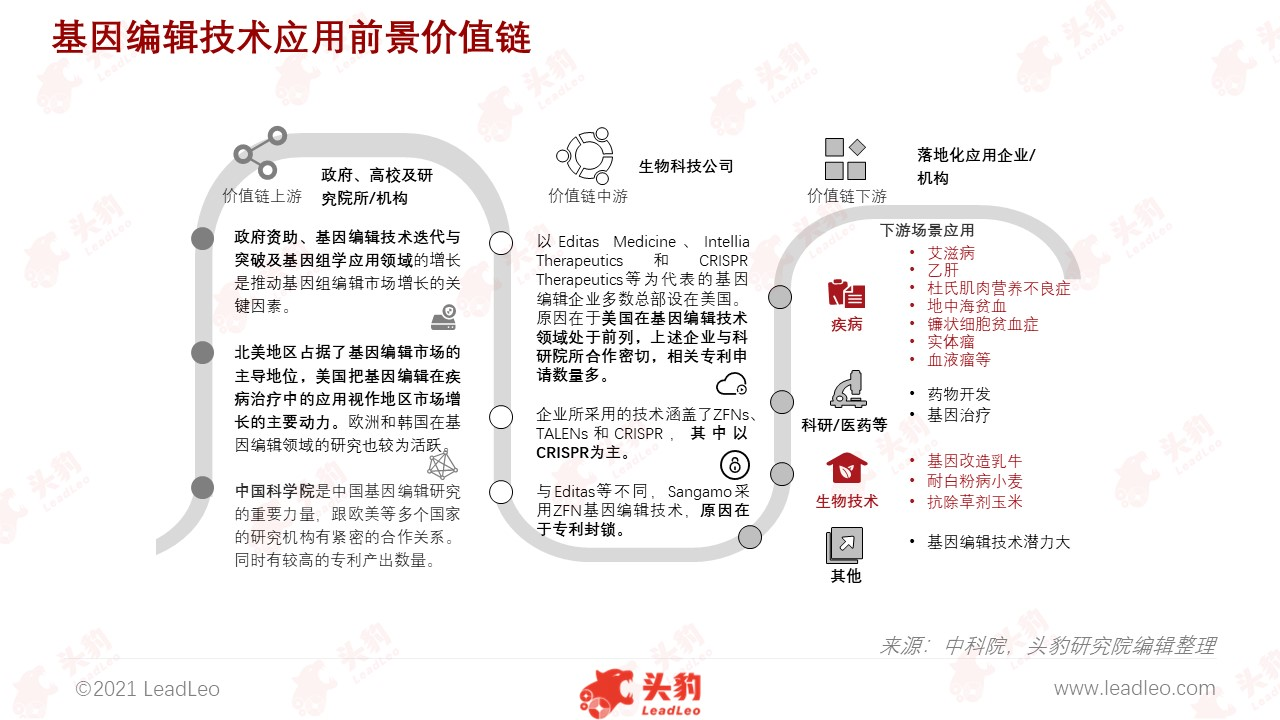
基因编辑技术在农业、畜牧业及医学领域有广阔的应用空间,在技术的持续拓展及延伸下,基因编辑技术将带来巨大的社会价值与经济价值。
在畜牧业/农业等生物技术领域,基因组编辑技术可以用来改良动植物品种,提供高产、优质、安全的食品。
在疾病防治和精准医疗等医学领域,基因编辑技术当前主要被用于尚无有效治疗方法、严重威胁生命的疾病。同时,基因编辑技术有望为近6,000种尚无有效治疗方法的人类遗传疾病带来治疗方法,乃至治愈希望。
临床探索
基因编辑疗法是基因编辑技术的治疗模式,以期积极地改变患有严重威胁生命疾病的患者的生活。大多数基因编辑疗法专注于单基因罕见病和肿瘤免疫治疗方面的应用,但学术界已开始拓展更广泛的应用领域。
CRISPR/Cas技术在基因编辑的临床数量增加,基因编辑技术相关的临床试验正在推动包括眼疾、遗传性疾病及肿瘤在内的多个治疗领域的发展。例如,Sangamo Therapeutics开发的ST-400和BIVV003(临床I/II期)通过编辑BCL11A来增强胎儿血红蛋白;Editas Medicine和Allergan开发的EDIT-101(临床I/II期)使用CRISPR–Cas9来剪切Leber先天性黑蒙症10型(LCA10)失明患者的一部分突变CEP290,从而迫使机体产生功能蛋白,达到恢复视力的效果。
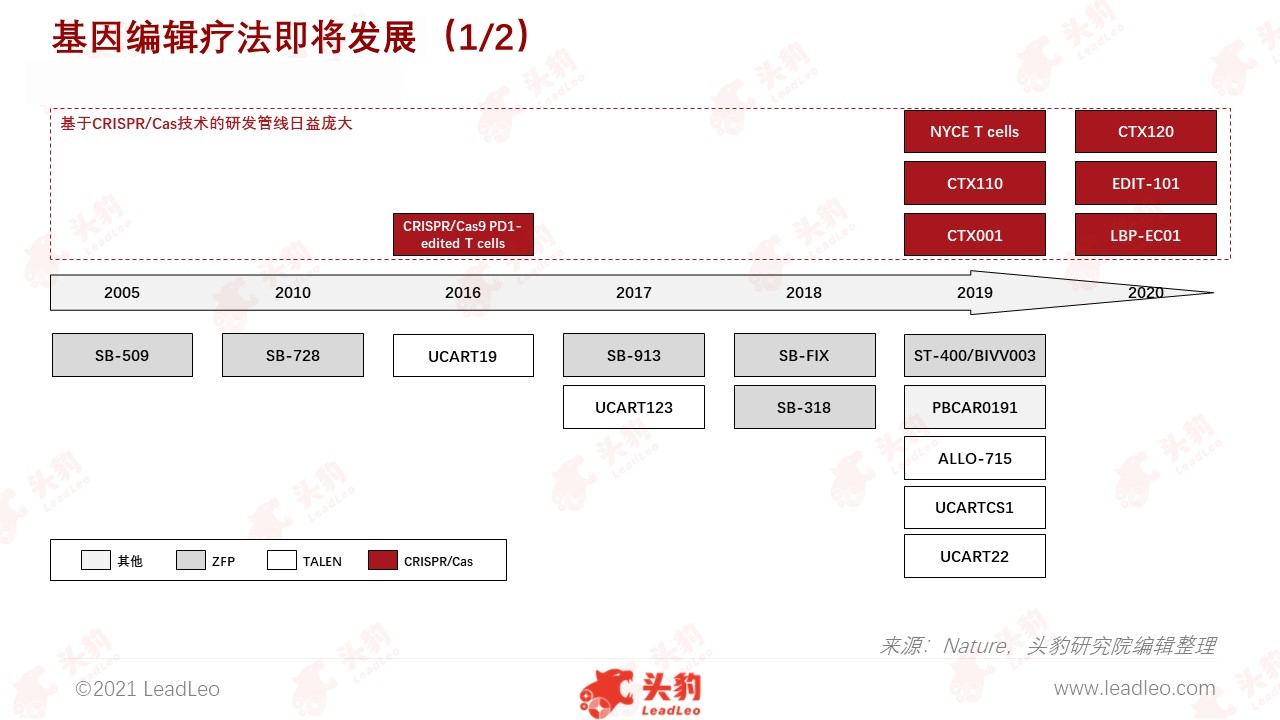
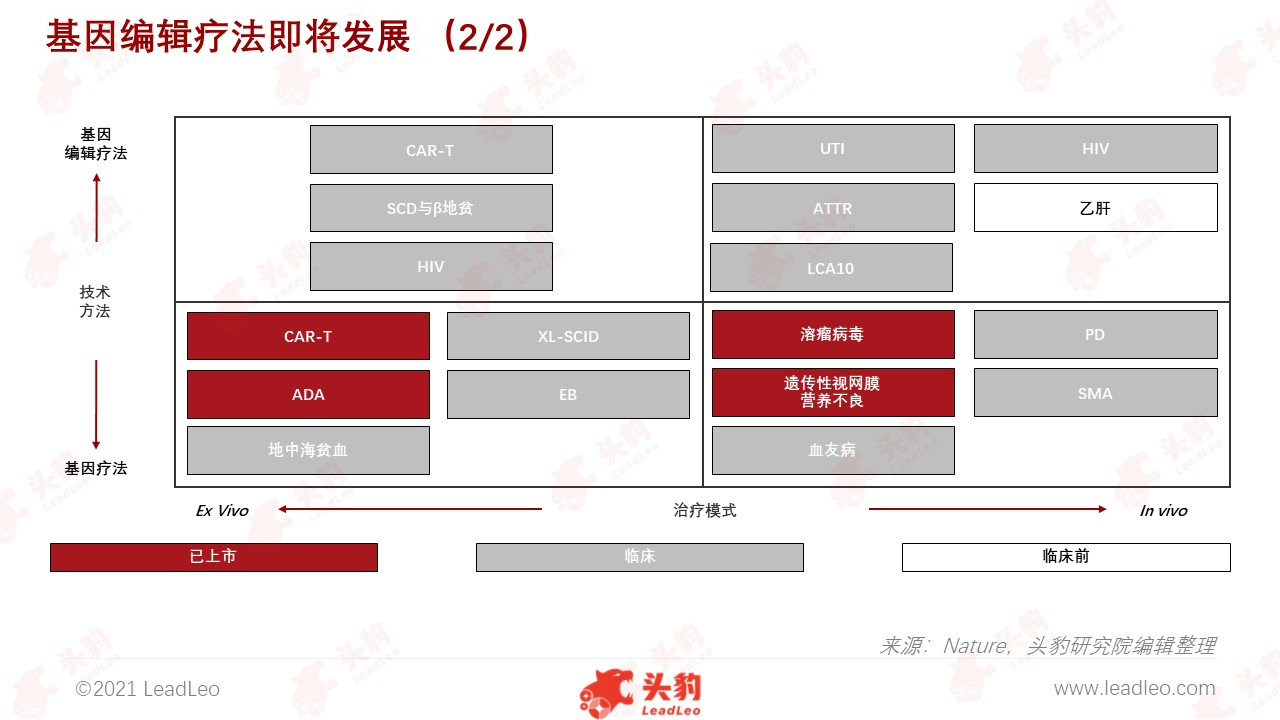
结合基因编辑疗法的特点,在梳理基因编辑疗法在研/已上市的管线后可见,基于基因编辑技术的体外疗法目前主要在镰刀型细胞贫血症(SCD)与β地中海贫血疾病领域,ZFN技术与CRISPR技术也均有涉及,目前处于临床研究阶段。
边界与红线
国际共识认为,基因编辑绝不能用于生殖目的。2020年,专家学者在NIH发布《Experts Conclude Heritable Human Genome Editing Not Ready for Clinical Applications》,要求国际暂停人类遗传性或种系基因组编辑的临床用途。
2021年3月16日,国家卫生健康委官网就《涉及人的生命科学和医学研究伦理审查办法(征求意见稿)》公开征求意见,其中指出,所有涉及人的生命科学和医学研究活动,均应当接受伦理审查。除此前规定的医疗卫生机构,高等学校、科研院所等开展涉及人的生命科学和医学研究伦理审查工作也纳入应当接受伦理审查范围中。(头豹研究院 郝世超)
本文仅代表作者观点,不代表本站立场。
《中国医药报》社版权所有,未经许可不得转载。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
为你推荐